FDA نخستین ژندرمانی سلولی برای بیماران پروانهای را تأیید کرد
تاریخ انتشار :
چهارشنبه ۱۰ ارديبهشت ۱۴۰۴ ساعت ۲۲:۳۸
کد مطلب : ۱۸۷۰۶
سالمخبر: شرکت Abeona Therapeutics موفق شد پس از یک سال تلاش و اصلاح درخواست خود، مجوز سازمان غذا و داروی آمریکا (FDA) را برای نخستین ژندرمانی سلولی ویژه یک بیماری ژنتیکی نادر پوستی دریافت کند.
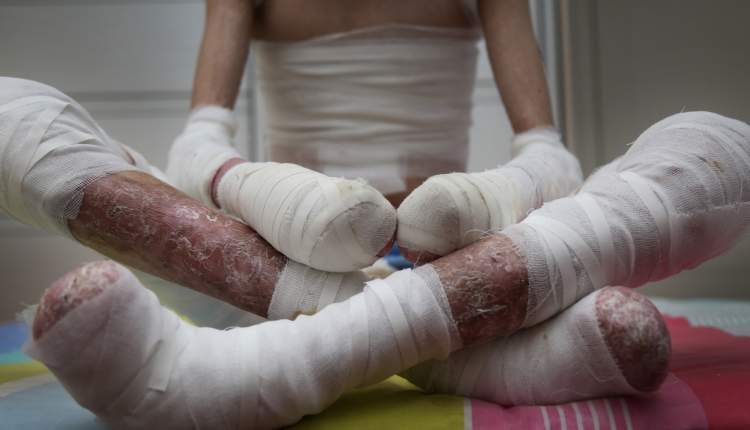
به گزارش سالمخبر به نقل از رویترز، این درمان که Zevaskyn نام دارد، برای بزرگسالان و کودکان مبتلا به دیستروفی اپیدرمیولیز بولوسای راجعه (RDEB) تأیید شده است. این بیماری ژنتیکی نادر باعث ایجاد زخمهای دردناک و گسترده روی پوست بیماران میشود و در برخی موارد تا ۸۰ درصد از سطح بدن را درگیر میکند. این زخمها علاوه بر درد شدید، منجر به عوارض جدی دیگری نیز میشوند.
تأیید Zevaskyn نقطه عطفی مهم برای Abeona به شمار میرود، به ویژه پس از آنکه سال گذشته FDA درخواست قبلی این شرکت را رد کرده بود. اکنون با اخذ این مجوز، Abeona رسماً وارد عرصه تجاریسازی ژندرمانی شده است.
Zevaskyn یک درمان سلول-پایه و خودی (autologous) است؛ بدین معنا که سلولهای خود بیمار استخراج، اصلاح ژنتیکی شده و سپس برای ترمیم بافت آسیبدیده به بدن بازگردانده میشوند. این روش بهطور مستقیم به رفع نقص ژنتیکی زمینهای بیماران مبتلا به RDEB میپردازد و میتواند کیفیت زندگی آنها را به شکل قابل توجهی بهبود بخشد.
رئیس Abeona در بیانیهای اعلام کرد: «تأیید Zevaskyn گامی بزرگ برای بیماران و خانوادههایی است که سالها منتظر درمان مؤثری برای این بیماری دردناک بودهاند. ما متعهد به عرضه سریع این درمان به بازار هستیم.»
با این تأیید، Zevaskyn به نخستین ژندرمانی سلولی برای درمان RDEB در آمریکا تبدیل شده است و راه را برای توسعه بیشتر روشهای درمانی مشابه برای سایر بیماریهای ژنتیکی هموار میکند.
به گزارش سالمخبر به نقل از رویترز، این درمان که Zevaskyn نام دارد، برای بزرگسالان و کودکان مبتلا به دیستروفی اپیدرمیولیز بولوسای راجعه (RDEB) تأیید شده است. این بیماری ژنتیکی نادر باعث ایجاد زخمهای دردناک و گسترده روی پوست بیماران میشود و در برخی موارد تا ۸۰ درصد از سطح بدن را درگیر میکند. این زخمها
تأیید Zevaskyn نقطه عطفی مهم برای Abeona به شمار میرود، به ویژه پس از آنکه سال گذشته FDA درخواست قبلی این شرکت را رد کرده بود. اکنون با اخذ این مجوز، Abeona رسماً وارد عرصه تجاریسازی ژندرمانی شده است.
Zevaskyn یک درمان سلول-پایه و خودی (autologous) است؛ بدین معنا که سلولهای خود بیمار استخراج، اصلاح ژنتیکی شده و سپس برای ترمیم بافت آسیبدیده به بدن بازگردانده میشوند. این روش بهطور مستقیم به رفع نقص ژنتیکی زمینهای بیماران مبتلا
رئیس Abeona در بیانیهای اعلام کرد: «تأیید Zevaskyn گامی بزرگ برای بیماران و خانوادههایی است که سالها منتظر درمان مؤثری برای این بیماری دردناک بودهاند. ما متعهد به عرضه سریع این درمان به بازار هستیم.»
با این تأیید، Zevaskyn به نخستین ژندرمانی سلولی برای درمان RDEB در آمریکا تبدیل شده است و راه را برای توسعه بیشتر روشهای درمانی مشابه برای سایر بیماریهای ژنتیکی هموار میکند.